プロテインキナーゼ阻害の検定 (I)
(担当:上原至雅)
チロシンキナーゼ阻害剤はがん分子標的治療薬の草分け的存在である。EGF受容体阻害剤ゲフィチニブやBcr-Abl阻害剤イマチニブはがん化学療法に革新的な進歩をもたらした。しかし、近年これらの分子標的薬に対する耐性化が問題となっている。がん分子標的治療のさらなる進展のためには、耐性克服は乗り越えなければならない課題の一つである。本評価系では、阻害剤感受性EGF受容体(EGFR WT、EGFR L858R)、阻害剤感受性Ablに加え、阻害剤耐性変異体(EGFR T790M/L858R、Abl T315I)、EGFRシグナルをバイパスするHGF受容体(Met)、VEGF受容体(Flt-1)の全7種類のキナーゼに対する阻害活性をin vitroキナーゼ反応によって評価する。
【方法】
阻害剤感受性EGFR野生型(WT)及びL858R変異体、阻害剤耐性EGFR T790M/L858R変異体、Met、阻害剤感受性Abl、阻害剤耐性Abl T315I変異体、Flt-1のキナーゼドメインの組み換えタンパク質を酵素として用いる。各酵素(50-100 ng/ 50μL) にサンプル化合物を添加し、25℃で30分間プレインキュベートする。ビオチン化標識基質ペプチド(poly Glu-Tyr)とATPをプレインキュベート液に加え、25℃で30分間リン酸化反応行わせる。EDTA添加により反応を停止させ、アビジンでコートされた96ウェルプレートに反応液を加えてビオチン化基質を結合させる。基質のリン酸化レベルを抗リン酸化チロシン抗体を用いたELISAによって測定する。本評価系では、ポジティブコントロールとしてゲフィチニブ(EGFR WT, L858R)、スタウロスポリン(EGFR T790M/L858R)、SU11274 (Met)、イマチニブ(Abl)、Aurora kinase inhibitor(Abl T315I)、VEGFR inhibitor II(Flt-1)を用いる。
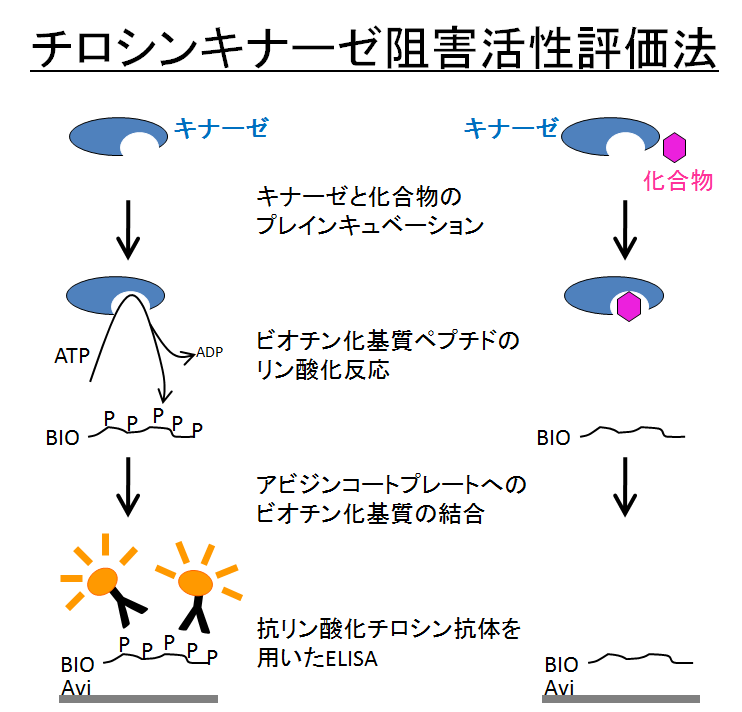
【活性の評価】
まず、サンプル化合物は最終濃度10μMで阻害活性を測定する。阻害活性の認められた化合物については、10倍希釈系列を作成し再度阻害活性を測定し、50%阻害濃度を求める。50%阻害濃度が1μM以下のものを陽性と判定する。






